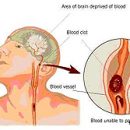
K dnešnému dňu je poranenie mozgu (CMT) jedným z najbežnejších druhov neurologickej patológie a je významným lekárskym a sociálno-ekonomickým problémom pre všetky segmenty obyvateľstva.
Obsah
V rozvinutých krajinách existuje stabilný rast neurotraumamizmu. Takže v krajinách Európy je 150 zaregistrovaných ročne–300 prípadov CHMT na 100 tisíc. Populácia. V USA, len 2003. Viac ako 1,5 milióna CMT. V Rusku, táto hodnota dosiahne 4 prípady na 1 tisíc. Ľudský. Najdôležitejším problémom v lekárskych podmienkach je, že významný počet obetí sa následne rozvíja tzv. Dôsledky odloženej CMT, často interpretované v rámci traumatickej encefalopatie. Medzi najbežnejšie syndrómy, ktoré určujú úroveň prispôsobenia sociálno-domácnosti a kvalita života pacientov, sú intelektuálne unikátne porušovanie. Posttraumatické kognitívne poruchy sa izolujú v 29,4% všetkých pacientov s následkami CHMT a v kombinácii s inými syndrómami — Y 35,7%. Všeobecne platí, že medzi dôsledkami odložených CMT kognitívnych porúch ako syndróm sa nachádza v 65,1% prípadov.
Patogenéza vývoja posttraumatických kognitívnych porúch je veľmi zložitá a mnohostranná. Ako hlavné faktory, ktoré môžu viesť k vytvoreniu kognitívneho deficitu v akútnom období, považujeme obe priame mechanické poškodenie mozgových tkanív a sprostredkovaný účinok určitých patofyziologických procesov vyplývajúcich z CHT, ako je opuch opuchu mozgu, Narušenie alkoholu, hemodynamiky a Dr. Zároveň je známe, že pokiaľ ide o prípady poruchy funkcií intelektuálneho jedla, je zachovaný dlhý čas alebo je trvalý charakter. U iných pacientov sa objavujú vo vzdialenom období zranenia a majú výrazný trend smerom k progresii. Mechanizmus výskytu takýchto porušení nie je študovaný v nápravnom prostriedku. Získané údaje naznačujú, že patologické faktory ovplyvňujú nervovú bunku v akútnom období, prispievajú k vzniku kaskády biochemických posunov v neurónoch, čo vedie k rozvoju dystrofických procesov a znížiť účinnosť synaptickej prevodovky.
V konečnom dôsledku existuje porušenie procesov šírenia informácií v neuronálnych sieťach, ktoré sa považujú za jeden z hlavných aspektov tvorby kognitívnych porušení. Počet výskumných pracovníkov si všimol určitú podobnosť patogenetických mechanizmov na vývoj kognitívnych porúch v CMT a vaskulárnych mozgových léziách. Okrem toho je možná úloha poranenia mozgu je znázornená ako odpaľovač neurodegeneratívnych ochorení, najmä Alzheimerovej choroby. V súčasnosti predstavuje niekoľko patofyziologických procesov významnú úlohu pri vytváraní posttraumatických kognitívnych porúch.
Jedným z týchto procesov je vývoj «Glutamát EXIANTOXICIE». Vo fyziologických podmienkach, glutamát pôsobí ako jeden z najdôležitejších vzrušujúcich mediátorov centrálneho nervového systému, ktorý sa zúčastňuje na implementácii procesov neuronálnej plasticity a integračných funkcií mozgu. V cerebrálnej kôre a hipokampe sa pozorovalo významné množstvo glutamanthergických receptorov. Zároveň sa pozorujú s patológiou, prebytočné emisie glutamátu, ktoré v týchto podmienkach má toxický účinok na neuronálne štruktúry, ktoré prispievajú k aktivácii glutamát-vápenatých kaskádových reakcií, čo vedie k nekontrolovanému zvýšeniu koncentrácie intracelulárneho vápnika , ktorý má negatívny vplyv na ponuku buniek energie. Ukázalo sa, že za podmienok ischémie v tkanivách existuje výrazný nárast úrovne tvorby voľných radikálov, ktoré tiež prispieva k nadmernému intracelulárnej akumulácii vápnika.
Mozog je veľmi citlivý na pôsobenie voľných radikálov. V podmienkach prevahy oxidačných systémov nad antioxidantom, tvorba tzv. Oxidačného napätia. V tomto prípade sa aktivuje hydrolýza fosfolipázy a bunkové membrány sú degradáciou, vrátane mitochondriálneho. Eliminácia rozvíjajúcich sa porúch je predpokladom úspešného riadenia pacienta s posttraumatickým kognitívnym poškodením. S týmito pozíciami je vhodné vymenovanie takéhoto lieku ako noopept s takýmito vlastnosťami. Noopept — N-fenyl-acetyl-L-prolyglycín etylester — Nový domáci pôvodný dipeptid vytvorený vo farmakológii. V.V.Zasakova Ramne. Podľa údajov získaných v priebehu experimentálnych štúdií má NOPEPT NOOTROPICKÉ A Neuroprotektívne vlastnosti. Liečivo v jej štruktúrnych konformačných charakteristík je podobné piracetamu a vazopresínom. Vývoj tohto lieku sa uskutočnil ako súčasť existujúcej myšlienky, že niektoré regulačné peptidy majú významný vplyv na mechanizmy pamäte a školenia.
Základom vysvetlenia pôsobenia Noopept je hypotézou, že bázická liečivo tejto skupiny piracetamu je analóg peptidového ligandu na špecifické nootropné receptory, podobne ako jeho vlastnosti s metabolitmi vazopresínu. Noopept je prospešný od vazopresínu, pretože je schopný ukazovať aktivitu so systémom, vrátane orálneho podávania. Počas štúdií bola ukázaná vysoká biologická dostupnosť lieku pre mozgové tkanivá, ako aj jeho nízka toxicita. Štúdium v experimente na laboratórnych zvieratách umožnilo stanoviť, že použitie liekových dávok, od 2 do 20-krát vyššie ako nootropné, nespôsobuje poškodenie vnútorných orgánov, nemá významné porušenia hematologických a biochemických ukazovateľov. Pri vykonávaní niekoľkých klinických štúdií sa tiež zobrazuje vysoká bezpečnosť liečiva a jeho dobrú tolerovateľnosť. V priebehu výskumu sa zistilo, že Noopept má komplexný mechanizmus akcie.
Po prvé, má nootropický účinok spojený so skutočnosťou, že jedným z aktívnych metabolitov Noopept je cykloprolglycín, ktorý je vo svojej štruktúre podobný endogénnemu cyklickému dippaotidu, ktorý má protizikovú aktivitu.
Po druhé, Noopept je schopný zvýšiť stabilitu mozgového tkaniva na škodlivé nárazy, ako je zranenie, hypoxické, elektrosuskulárne a toxické lézie, ktoré charakterizuje neuroprotektívny účinok tohto lieku. Po tretie, je ukázané, že možnosť noopept, aby sa zabránilo podmienkam činností toxických koncentrácií glutamátu a aktívnych foriem kyslíkovej smrti neurónov v tele kortexu mozgovej kôry a cerebellum. Okrem toho experiment ukázal schopnosť znížiť toxický účinok B-amyloidu, zvýšiť produkciu anti-mylideových protilátok, modulovať prevádzku cholinergných receptorov, ako aj stimuláciu expresiu neurotrofických faktorov (BDNF a NGF) v Cerebrálna kôra a hipokamp.
Relevantnosť problému posttraumatických kognitívnych porušení, platnosti používania Noopept, pričom zohľadní prítomnosť bodov na žiadosť na neurochemickej úrovni za dôsledkoch CHT, ako aj predbežného, vrátane experimentálneho a \ t Klinická účinnosť lieku bola dôvodom tejto štúdie.
Účelom štúdie bolo vyhodnotiť účinnosť, ako aj bezpečnosť používania liečiva do pacientov so svetlými posttraumatickými kognitívnymi poruchami. Štúdia bola vykonaná na osobitne vyvinutej protokolu a dodržaná všetky požiadavky príslušnej klinickej praxe (GCP) prijatej v Ruskej federácii. Štúdia zahŕňala pacientov, ktorí spĺňajú kritériá na zaradenie, po povinnom podpísaní informovaného súhlasu.
30 pacientov vo veku 19 rokov sa zúčastnilo štúdia–66 rokov (priemerný vek 33 rokov±10,3 roky), ktorý utrpel Chht (otrasus alebo zranenie mozgu svetla) najmenej pred 6 mesiacmi a s narušením funkcií intelektuálneho jedla spojeného s týmto stavom zodpovedajúcim kritériám pre miernu syndrómu kognitívnych porúch. Všetci pacienti zodpovedali kritériám pre syndróm miernych kognitívnych porušení a ich kognitívne poruchy boli pôvodne hodnotené v 25 alebo viacerých bodoch na mini-duševnej skúšobnej meradle (MMSE).
Kritériá výnimiek z výskumu boli: prítomnosť súbežných ťažkých alebo nestabilných somatických ochorení, ktoré ohrozujú život pacienta, prítomnosť klinicky významných iných (okrem syndrómu mierneho kognitívnych porušení s dôsledkami CHF) neurologických alebo duševných porúch, \ t Prítomnosť hrubého motorového alebo zmyslového defektu alebo iných porúch, ktoré sťažujú, že by to sťažilo, bolo by vykonávanie neuropsychologickej štúdie alebo iné štúdie stanovené protokolom, históriu mŕtvice alebo diskorulačnej encefalopatie štádium III, súčasné vodivé terapie s inými vazoaktívnymi, metabolické alebo psychotropné lieky s overeným kognitívnym účinkom, neznášanlivosťou na liečivo pod štúdiom, tehotenstvo a dobu laktácie.
Pri práci na objektiváciu získaných údajov boli použité
Nasledujúce metódy:
1) Posúdenie neurologického stavu;
2) Stručná škála mentálneho stavu — Mmse;
3) Hamiltonové váhy na posúdenie depresie;
4) Skúšobná batéria pre frontálnu dysfunkciu — Batéria čelnej hodnotenia (Fab);
5) Sledujte test kreslenia;
6) Skúška 10 slov;
7) Skúška Schulte;
8) Rozsah ratingu všeobecného klinického dojmu zmeny — Klinik’S Interview Založený dojem zmien plus (CIBIC PLUS);
9) Metódy neuroviarizácie: počítačová alebo magnetická rezonančná tomografia.
Posúdenie na stupnici všeobecných klinických skúseností stanovených na posúdenie stavu pacienta na liečbu a hodnotenie závažnosti zmien v pozadí liečby. Účasť lekára pred začiatkom liečby sa posúdenie stavu pacienta na základe analýzy porúch na 7-bodovej stupnici, odhad klinického obrazu choroby, monitorovania pacienta, stav duševnej gule Pacient, správanie, stav sociálno-domácich funkcií.
Na začiatku štúdie sa vykonalo skríningová návšteva, na ktorej bol dodržiavanie pacienta určené kritériami zaradenia. Potom v prípade zhody pacienta, protokol podpisuje informovaný súhlas. Táto návšteva tiež hodnotila výsledky elektrokardiogramov, laboratórnych a neurovalizačných metód výskumu. Potom sa odhadoval neurologický stav, sa uskutočnilo základné neuropsychologické testovanie s cieľom určiť počiatočnú úroveň stavu kognitívnych funkcií.
Počnúc druhým dňom prerezávacej návštevy pacienti dostávali noopept po dobu 10 mg 2-krát denne počas 60 dní. V budúcnosti sa vyhodnotenie účinnosti terapie uskutočnilo na 30. a 60. dňoch liečby. Plán udalostí je uvedený v tabuľke.
V našej štúdii, priemerné obdobie po urážke bolo 7±3,8 roka. Všetkých 30 pacientov, ktorí vstúpili do štúdie, pôvodne malo ľahké porušovanie na stupnici všeobecného klinického dojmu zmenu (CIBIC PLUS). Počas skríningovej návštevy všetky skúmané pacienti prezentovali sťažnosti o znížení pamäte, koncentrácie pozornosti, zníženie účinnosti vykonávania denných činností, všeobecnej slabosti, zvýšenej únavy. Okrem toho niektorí pacienti prezentovali ďalšie sťažnosti: na bolesti hlavy (43,3%), ťažkosti s plánovaním rôznych aktivít (40%), poruchy spánku (26,7%), nestabilita nálady (23,3%). Počas neurologického vyšetrenia hrubého porušenia neboli zistené. V 53,3% pacientov sa vyskytli rozptýlené príznaky vo forme izolovaných mikrosibptómov, 13,3% — Porušenie koordinátora svetla. Na rovnakom počte pozorovaných bilaterálnych patologických plastových reflexov (Rossolimo, Vartenberg). Všetci pacienti mali príznaky astenického syndrómu. 53,3% pozorovali príznaky vegetatívne-vaskulárnej nestability.
Štúdium kognitívnych funkcií pacientov uskutočnených v dynamike ukázalo, že podľa výsledkov meradle MMSE boli spoľahlivé rozdiely s počiatočnou úrovňou ukázané 30 dní po začiatku liečby. Predovšetkým pred prijatím lieku bolo priemerné skóre 26,5±0,94; 1 mesiac od začiatku terapie — 27.6±0,99 bodov (p<0,01). Zároveň 60 dní od začiatku terapie bolo priemerné skóre v tejto mierke 27,7±1,09, vyznačujúci sa tým, že absencia ďalšieho spoľahlivého zlepšenia (p>0,05) a iba tendencia na zníženie kognitívnych porúch. Dynamika neuropsychologických indikátorov na stupnici MMSE je prezentovaná v ryži. jeden.
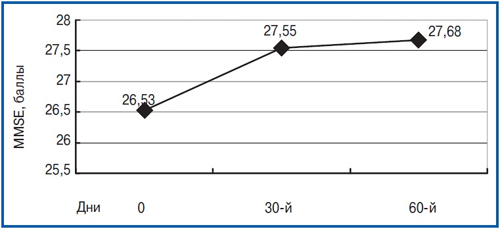
Obrázok 1
Zaujímavosťou bola skutočnosť, že v štruktúre škály MMSE bola najvýznamnejšia zlepšenie indikátorov získaná subshkale «Pozornosť», charakterizuje v určitej miere stav neurodynamických procesov trpiacich TBMC (P<0,01), ako aj na subshkale «Pamäť» (R<0,05). Na stupnici batérií testov na vyhodnotenie frontálnej dysfunkcie Fab spoľahlivé rozdiely v období pozorovania v dynamike neboli k dispozícii (na počiatočnej návšteve — 15.9±0,78 bodov, o 60 dní neskôr — 16.8±0,87, p = 0,27). Skúška skúšky výkresu hodiny s 10-bodovým odhadom na zdrojovej návšteve sa zvyčajne odhaduje na 9–10 bodov a proti pozadia liečby významných zmien sa nepodarilo. Samozrejme, údaje získané na základe hodnotenia výsledkov vzorky Schulte, ktorý bol vykonaný na všetkých 3 návštevách. Komplexná odhadovaná vzorka s použitím 5 postupne prezentovaných tabuliek pacientov najviac umožňuje charakterizovať takéto neurodynamické zmeny ako zhoršenie koncentrácie pozornosti, zvýšené vyčerpanie mentálnych procesov a pozornosť nestability. Tieto zmeny v určitom rozsahu boli charakterizované väčšinou pacientov na skríningových návštevách. Priemerná skúšobná doba pre každú z piatich prezentácií v prvej návšteve bola 45,5±6,24 S. Po 2 mesiacoch po začatí liečby sa čas znížil na 40,2±5,20 S, ktoré charakterizovali významné zlepšenie koncentrácie pozornosti (p<0,05). Dynamika času vzorky Schulte je prezentovaná v ryži. 2.
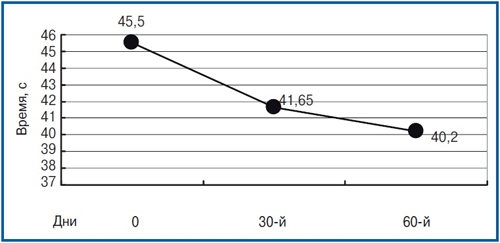
Obrázok 2
Ako možno vidieť z grafu v ryži. 2, najvýznamnejšie zníženie času stráveného na vykonávanie vzoriek ukázali pacienti 30 dní po začiatku liečby. Uznávajúc si pozitívnu dynamiku pretrváva aj v 2. mesiaci liečiva a bol charakterizovaný ešte výraznejší pokles v testovacom čase s menej významnou stabilizáciou zlepšenia ako na stupnici MMSE.
Posúdenie na stupnici všeobecných klinických skúseností stanovených na posúdenie stavu pacienta na liečbu a hodnotenie závažnosti zmien v pozadí liečby. Účasť lekára pred začiatkom liečby sa posúdenie stavu pacienta na základe analýzy porúch na 7-bodovej stupnici, odhad klinického obrazu choroby, monitorovania pacienta, stav duševnej gule Pacient, správanie, stav sociálno-domácich funkcií.
Na začiatku štúdie sa vykonalo skríningová návšteva, na ktorej bol dodržiavanie pacienta určené kritériami zaradenia. Potom v prípade zhody pacienta, protokol podpisuje informovaný súhlas. Táto návšteva tiež hodnotila výsledky elektrokardiogramov, laboratórnych a neurovalizačných metód výskumu. Potom sa odhadoval neurologický stav, sa uskutočnilo základné neuropsychologické testovanie s cieľom určiť počiatočnú úroveň stavu kognitívnych funkcií.
Počnúc druhým dňom prerezávacej návštevy pacienti dostávali noopept po dobu 10 mg 2-krát denne počas 60 dní. V budúcnosti sa vyhodnotenie účinnosti terapie uskutočnilo na 30. a 60. dňoch liečby. Plán udalostí je uvedený v tabuľke.
| Výskumné metódy | I | II | Iii |
| Pozadie | 30. deň | 60. deň | |
| Kolekcia hodnotenia duševného stavu (MMSE) | V | V | V |
| Vyhodnotenie čelnej dysfunkcie (Fab) | V | V | |
| Skúšobné hodiny 10 – Palelný odhad | V | V | |
| Rozsah všeobecného klinického dojmu (CGI) | V | V | |
| Skúška 10 slov | V | V | |
| Vzorka schulte | V | V | V |
| Hamilton | V | ||
| Vyhodnotenie nežiaducich javov a vedľajších účinkov | V | V |
Obrázok 3
V našej štúdii, priemerné obdobie po urážke bolo 7±3,8 roka. Všetkých 30 pacientov, ktorí vstúpili do štúdie, pôvodne malo ľahké porušovanie na stupnici všeobecného klinického dojmu zmenu (CIBIC PLUS). Počas skríningovej návštevy všetky skúmané pacienti prezentovali sťažnosti o znížení pamäte, koncentrácie pozornosti, zníženie účinnosti vykonávania denných činností, všeobecnej slabosti, zvýšenej únavy. Okrem toho niektorí pacienti prezentovali ďalšie sťažnosti: na bolesti hlavy (43,3%), ťažkosti s plánovaním rôznych aktivít (40%), poruchy spánku (26,7%), nestabilita nálady (23,3%). Počas neurologického vyšetrenia hrubého porušenia neboli zistené. V 53,3% pacientov sa vyskytli rozptýlené príznaky vo forme izolovaných mikrosibptómov, 13,3% — Porušenie koordinátora svetla. Na rovnakom počte pozorovaných bilaterálnych patologických plastových reflexov (Rossolimo, Vartenberg). Všetci pacienti mali príznaky astenického syndrómu. 53,3% pozorovali príznaky vegetatívne-vaskulárnej nestability.
Štúdium kognitívnych funkcií pacientov uskutočnených v dynamike ukázalo, že podľa výsledkov meradle MMSE boli spoľahlivé rozdiely s počiatočnou úrovňou ukázané 30 dní po začiatku liečby. Predovšetkým pred prijatím lieku bolo priemerné skóre 26,5±0,94; 1 mesiac od začiatku terapie — 27.6±0,99 bodov (p<0,01). Zároveň 60 dní od začiatku terapie bolo priemerné skóre v tejto mierke 27,7±1,09, vyznačujúci sa tým, že absencia ďalšieho spoľahlivého zlepšenia (p>0,05) a iba tendencia na zníženie kognitívnych porúch. Dynamika neuropsychologických indikátorov na stupnici MMSE je prezentovaná v ryži. jeden. Zaujímavosťou bola skutočnosť, že v štruktúre škály MMSE bola najvýznamnejšia zlepšenie indikátorov získaná subshkale «Pozornosť», charakterizuje v určitej miere stav neurodynamických procesov trpiacich TBMC (P<0,01), ako aj na subshkale «Pamäť» (R<0,05). Na stupnici batérií testov na vyhodnotenie frontálnej dysfunkcie Fab spoľahlivé rozdiely v období pozorovania v dynamike neboli k dispozícii (na počiatočnej návšteve — 15.9±0,78 bodov, o 60 dní neskôr — 16.8±0,87, p = 0,27). Skúška skúšky výkresu hodiny s 10-bodovým odhadom na zdrojovej návšteve sa zvyčajne odhaduje na 9–10 bodov a proti pozadia liečby významných zmien sa nepodarilo.
Samozrejme, údaje získané na základe hodnotenia výsledkov vzorky Schulte, ktorý bol vykonaný na všetkých 3 návštevách. Komplexná odhadovaná vzorka s použitím 5 postupne prezentovaných tabuliek pacientov najviac umožňuje charakterizovať takéto neurodynamické zmeny ako zhoršenie koncentrácie pozornosti, zvýšené vyčerpanie mentálnych procesov a pozornosť nestability. Tieto zmeny v určitom rozsahu boli charakterizované väčšinou pacientov na skríningových návštevách. Priemerná skúšobná doba pre každú z piatich prezentácií v prvej návšteve bola 45,5±6,24 S. Po 2 mesiacoch po začatí liečby sa čas znížil na 40,2±5,20 S, ktoré charakterizovali významné zlepšenie koncentrácie pozornosti (p<0,05). Dynamika času vzorky Schulte je prezentovaná v ryži. 2. Ako možno vidieť z grafu v ryži. 2, najvýznamnejšie zníženie času stráveného na vykonávanie vzoriek ukázali pacienti 30 dní po začiatku liečby. Uznávajúc si pozitívnu dynamiku pretrváva aj v 2. mesiaci liečiva a bol charakterizovaný ešte výraznejší pokles v testovacom čase s menej významnou stabilizáciou zlepšenia ako na stupnici MMSE.